Vše o osmiu

Osmium - vzácný kov, patří do skupiny platiny. Byl objeven v Anglii jako výsledek pokusů o reakci platiny. Název osmium je uveden v řečtině a v překladu znamená „vůně“. Jaký je tento ušlechtilý kov? Jaké jsou jeho vlastnosti a jaké je jeho využití?

Dějiny
K objevu tohoto prvku došlo náhodou v roce 1803 anglickými chemiky Smithson Tennant a William H. Wollastan. V důsledku pokusů o reakci platiny na směs kyselin (sírové a dusičné) se ve vzniklé sraženině vyvinulo nepříjemné aroma, připomínající zápach chlóru a shnilé ředkve. Podobné experimenty provedli Colle-Descoti, Antoine de Fourcoy a Vauquelin ve Francii. V důsledku svého výzkumu našli neznámou látku také v nerozpustném sedimentu z platiny.



Tehdy neznámá látka dostala jméno kuřátko, ale pokusy Britů prokázaly, že jde o dvě podobné látky – iridium a osmium.
Objev těchto chemických prvků byl předložen Královské společnosti v Londýně Tennantovým písemným sdělením z 21. června 1804. V periodické tabulce chemických prvků Mendělejeva se kov nachází pod pořadovým číslem 76. Kov se nevyskytuje ve své čisté formě ve formě nugetů, proto je jeho chemický vzorec prezentován v rozpuštěné formě.


Prvek se získává z druhotných surovin v důsledku jeho oddělení od iridiových, platinových, platino-palladiových rud nebo měděných a niklových rud. Roční produkce celého prvku ve světě nepřesahuje velikost 1 tuny.


Místo narození
Největší světová naleziště stojí za povšimnutí takové zóny jako Uralské pohoří a Sibiř v Rusku, severní stát Aljaška a západní stát Kalifornie v Americe, Kanada v Severní Americe, Kolumbie v Jižní Americe a některé země jižní Afriky, Austrálie, Ostrov Tasmánie... V současné době se uvažuje o významném ložisku osmia Bushwell Complex v Jižní Africe, většina látky se tam těží. Vezmeme-li v úvahu, že největší ložiska kovu jsou v Jižní Africe, jsou světové ceny tohoto kovu vzácných zemin poměrně vysoké. Kazachstán je považován za jediného velkého vývozce osmia-187 na světě. Ačkoli Čína má zásoby platinové rudy, nemá významné množství osmia.


Látka je skladována v práškové formě a vzhledem k tomu, že se netaví ve formě krystalů, není možné na ni kvůli fyzikálním vlastnostem nalepit razítko. Pro výrobu ingotů z tohoto kovu se používá elektronový nebo obloukový ohřev z prášku, dále ohřev v kelímku.


Vlastnosti
Osmium vypadá jako stříbřitý namodralý kov. Je to jeden z nejhustších prvků, jeho hustota je 22600 kilogramů na metr krychlový, ale zároveň je hmota docela křehká, snadno se láme a drolí. Má vysokou měrnou hmotnost a je schopen zářit i při poměrně vysokých teplotních vlivech. Vzhledem k jeho parametrům a výrazné teplotě tavení je obtížné jej obrábět. V přírodě existuje ve formě sedmi izotopů, z nichž šest je považováno za stabilních, jedná se o osmium-184, osmium-187, osmium-188, osmium-189, osmium-190 a osmium-192. Laboratorně byly získány izotopy radioaktivních kovů s hmotnostními čísly od 162 do 197 a uměle byly získány i některé jaderné izomery.
Osmium svými vlastnostmi nepříznivě ovlivňuje všechny živé organismy.

Téměř všechny sloučeniny s tímto kovem způsobují poškození vnitřních orgánů, poruchy zraku a sluchu. Při otravě parami osmia může dojít k nevratným poruchám v těle a smrti. Vědci provedli pokusy na zvířatech, jejichž výsledkem byl rychlý rozvoj anémie, nedostatek normální funkce plic. Dospělo se k závěru, že se jedná o rychle se rozvíjející edém. Oxid osmičelý, který se používá v lékařství, je velmi žíravá látka. Má ten nejodpornější zápach na světě. Při otravě kůže trpí, mění barvu na zelenou nebo černou, často doprovázenou vředy a prasklinami, které se budou hojit velmi dlouho.

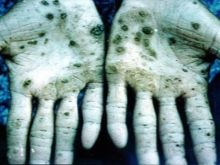

Nejvíce jsou ohroženi zaměstnanci výrobních provozů, kteří podle všech bezpečnostních norem pracují pouze v respirátorech a speciálním oděvu. Všechny nádoby obsahující oxid osmium jsou zapečetěny a skladovány v souladu s pravidly. Pro získání minerálů nevyanskitu se platina převádí na roztok pomocí aqua regia. Poté je výsledná sraženina vystavena působení zinku v 8násobném množství - taková slitina poměrně snadno přejde do práškového stavu, který je následně roztaven s peroxidem barya. Další fází je zpracování výsledné hmoty s aqua regia, destilace přes aparaturu pro oddělování oxidu osmičelého.

Působením na látku alkalickým roztokem se získá sůl. Je ovlivněn fyziologický roztok hyposiřičitan, v důsledku čehož se pomocí chloridu amonného vysráží kov již ve formě Fremyho soli. Sraženina se promyje, filtruje a kalcinuje. Výsledkem všech těchto akcí je houbovité osmium. Následně se čistí kyselinami, redukuje v elektrické peci pod proudem vodíku a ochladí. Tak získat vzorky osmia až 99,9 %.


Chemikálie
Vlastnosti tohoto prvku jsou z hlediska chemie úžasné. Nejzákladnější z nich jsou následující.
- Osmium vůbec nereaguje s alkáliemi a kyselinami. V reakci s alkalickými taveninami tvoří ve vodě rozpustné osmáty. Interakce se směsí kyseliny dusičné a chlorovodíkové dává extrémně pomalou reakci.
- Velmi toxický, dokonce i v mikroskopických dávkách. Obzvláště toxický je oxid osmičelý, který se uvolňuje z platiny.
- Je nemožné určit bod varu kovu, protože je zvláště žáruvzdorný.
- Kov v prášku snadno vstupuje do zahřívací reakce s takovými látkami: čistým kyslíkem, halogeny, kyselinou sírovou nebo dusičnou.
- V různých sloučeninách se získají oxidová čísla od -2 do +8. Nejběžnější jsou +2, +3, +4 a +8.
- Schopný tvořit klastrové sloučeniny.
- Hlavní minerály jsou příbuzné tuhým roztokům a jsou zastoupeny slitinami iridia s osmiem - jsou to sysertskit a nevyanskit. Kromě toho má syserskit jiný název - iridní osmium a nevyanskit - osmózní iridium.

Fyzický
Hustota osmia je přibližně 22,61 gramů na centimetr krychlový. Krystaly mají krásný stříbřitý lesk s různými odstíny od šedé po modrou. V ingotech se objevuje tmavě modrá barva, v prášku je fialová. Celý kov má stříbřitý lesk. Toxicita prvku brání jeho použití ve šperkařském průmyslu. Hlavní fyzikální vlastnosti jsou následující.
- Bod tání tohoto prvku je poměrně vysoký, tání je možné při teplotách přes 3000 stupňů Celsia.
- Kov nemá žádné magnetické vlastnosti.
- Úžasná pevnost. Slitiny s přídavkem tohoto kovu získávají zvýšenou odolnost proti opotřebení, trvanlivost, odolnost proti korozi a odolnost proti mechanickému namáhání.
- Bod varu je 5012 ºC.
- Mohsova tvrdost je 7.
- Tvrdost podle Vickerse je 3-4 GPa.

Aplikace
Kvůli značným nákladům na samotný prvek se tento kov zřídka používá v hromadné průmyslové výrobě. Osmium se používá především v chemickém průmyslu, kde se používá jako katalyzátor. Oxid osmičelý se používá v některých lécích. V laboratorních rozborech se používá k barvení živých tkání, zajišťuje zachování buněčné struktury.
V leteckém průmyslu se používá osmium v elektronickém vybavení zařízení pro leteckou a raketovou techniku, stejně jako ve výrobě nukleární zbraně. Kvůli nedostatku magnetických vlastností, kov se používá při výrobě značkových hodinek jako je Rolex. Slitina osmia s platinou se používá při tvorba chirurgických implantátů Jsou to kardiostimulátory nebo plicní chlopně.
Kromě toho se osmium používá v mikroskopii a k vytváření vysoce přesných přístrojů.



Zajímavosti
- Pod tlakem asi 770 GPa v osmiu interagují elektrony ve vnitřních orbitalech, struktura látky zůstává nezměněna.
- Osmium v horninách obsahuje půl procenta celkové hmoty rudních ložisek.
- Kvůli vysoké hustotě vzhled a skutečná hmotnost kovu se velmi liší. Takže 0,5litrová plastová láhev naplněná tímto kovovým práškem bude těžší než 10litrový kbelík naplněný vodou.
- Tento kov je v pěti nejvíce nákladné.
- Cena trojité unce osmia je obchodní tajemství, v otevřených zdrojích lze najít přibližnou cenu za 1 gram látky.
- Kvůli žáruvzdornosti osmia zapsaný v historii elektrické lampy. Vědec K. Auer von Welsbach z Německa navrhl nahradit uhlíkové vlákno v žárovce osmiovým vláknem. Ukázalo se, že žárovky jsou 3x méně energeticky náročné a osvětlení se výrazně zlepšilo. Pravda, brzy byl nahrazen běžnějším tantalem, který byl naopak nahrazen wolframem.
- Podobná situace nastala u vzácného kovu při výrobě čpavku. Metoda syntézy amoniaku, která se používá dodnes, vyvinutá v roce 1908 chemikem Fritzem Haberem z Německa, je nemožná bez použití katalyzátorů.Zpočátku používané katalyzátory vykazovaly své vlastnosti pouze za přítomnosti významných teplotních podmínek a neměly vysokou účinnost, takže hledání náhrady bylo velmi relevantní. Vědci z laboratoře Vyšší technické školy v Karlsruhe navrhli použít jako katalytický prvek jemně atomizované osmium. Výsledky testů potvrdily, že tento nápad stojí za to, katalytická teplota klesla o více než 100 ºC a výrazně se zvýšilo uvolňování amoniaku. Je pravda, že v budoucnu odmítli osmium, ale pomohl při řešení tak důležitého problému.

Osmium a další vzácné a jedinečné kovy hrají významnou roli v různých průmyslových odvětvích... I přes veškerou svou toxicitu zachraňuje životy a zdraví lidí.
Další informace o osmiu naleznete v následujícím videu.








